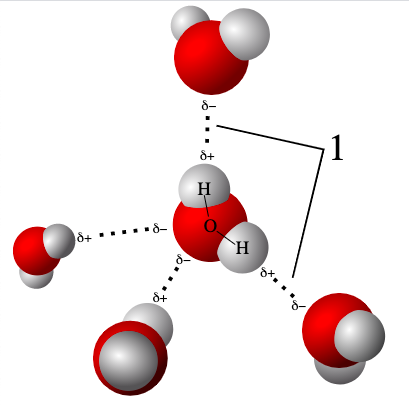
H2O তে H +ও OH-আয়ন থাকে এখানে OH-আয়ন কোথা থেকে আসে?
H2O মূলত একটি সমযোজী বন্ধনে তৈরি যৌগ:
অর্থাৎ দুইটি H পরমাণু ও একটি O তাদের একে ওপরের সাথে electron share করে যৌগ গঠন করেছে। আরও বিস্তারিত ভাবে বলা যায়, H এর একটি প্রোটন ও একটি ইলেকট্রন রয়েছে আর O এর কক্ষ পথে ৮ টি ইলেকট্রন ও ৮টি প্রোটন রয়েছে। সমযোজী বন্ধন ব্যাখ্যার জন্য ইলেকট্রনের সংখ্যাটা গুরুত্ব পূর্ণ কারণ H কে He (হিলিয়াম, ২) এর ন্যায় অধিক স্থায়ী ইলেকট্রন বিন্যাস অর্জন করার জন্য তার আরও একটি ইলেকট্রন প্রয়োজন অন্যদিকে O এর Ar (আর্গন , ১০) এর ন্যায় অধিকতর স্থায়ী ইলেকট্রন বিন্যাস অর্জনের জন্য আরও ২টি ইলেকট্রন প্রয়োজন তাই তারা একে ওপরের থেকে শেয়ার করার মাধ্যমে তাদের নিজ নিজ প্রয়োজনীয় ইলেকট্রন পেয়ে থাকে।
একে ওপরের সাথে যে বন্ধন এর সাহায্যে যৌগ গঠন করে থেকে সমযোজী যৌগ বলে। অর্থাৎ দুই H তারা একটি O এর এর থেকে ২টি ইলেকট্রন পেয়ে থাকে অন্য দিকে একটি O দুটি H থেকে ২টি এলেক্ত্রন শেয়ার করে বন্ধন তৈরি করে। এজন্য H2O বা পানির একটি অণু তৈরি করতে ২টি H ও একটি O পরমাণুর প্রয়োজন হয়।
এখন আমরা ব্যাখ্যা করব যে -OH আসলে কোঠা থেকে আসল। আসলে H2O কে পুরোপুরি সমযোজী যৌগ বলা হয় না কারণ পানির গঠন লক্ষ্য করলে বোঝা যায় যে, ইলেকট্রনগুলো H ও O এর মধ্যে সম ভাবে বণ্টন হয়নি কিছুটা আংশিক বলা যায়। অর্থাৎ অধিকতর ইলেকট্রন আসক্তি O এ দিকে ফলে O ঋণাত্মক চার্জ বহন করে এবং অধিকতর ধনাত্মক চার্জ H এর দিকে । তাই যখন আমরা অধিকতর তাপ ও চাপে তাদের মধ্যেকার বন্ধনকে ভাঙতে চেষ্টা করি তখন একটি H ধনাত্মক চার্জ দেখায় এবং OH মিলে ঋণাত্মক চার্জ দেখায়।
H2O কে মূলত পোলার সমযোজী যৌগ বলা হয়। পানির আসলেই একটি রহস্যময় অণু। কারণ পানির আরও অনেক চমকপ্রদ বৈশিষ্ট্য আছে যা আপনাকে চমকে দিবে।যেমন একটি পুকুরের বা যে কোন জলাশয়ের এমনকি এক গ্লাস জলের মধ্যেকার অণুগুলোও দীর্ঘদিন পর আলাদা আলাদা অণু হিসাবে পার্থক্য করা যায়। অর্থাৎ জলাশয়ের পানির অণু আর গ্লাসে রাখা পানির অণু আলাদা বৈশিষ্ট্য দেখায়।